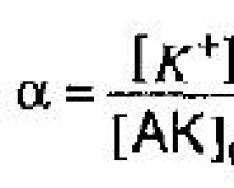Теорию электролитической диссоциации предложил шведский ученый С. Аррениус в 1887 году.
Электролитическая диссоциация - это распад молекул электролита с образованием в растворе положительно заряженных (катионов) и отрицательно заряженных (анионов) ионов.
Например, уксусная кислота диссоциирует так в водном растворе:
CH 3 COOH⇄H + +CH 3 COO - .
Диссоциация относиться к обратимым процессам. Но различные электролиты диссоциируют по-разному. Степень зависит от природы электролита, его концентрации, природы растворителя, внешних условий (температуры, давления).
Степень диссоциации α - отношение числа молекул, распавшихся на ионы, к общему числу молекул:
α=v´(x)/v(x).
Степень может варьироваться от 0 до 1 (от отсутствия диссоциации до ее полного завершения). Обозначается в процентах. Определяется экспериментальным путем. При диссоциации электролита происходит увеличение числа частиц в растворе. Степень диссоциации показывает силу электролита.
Различают сильные и слабые электролиты .
Сильные электролиты - это те электролиты, степень диссоциации которой превышает 30%.
Электролиты средней силы - это те, степень диссоциации которой делит в пределах от 3% до 30%.
Слабые электролиты - степень диссоциации в водном 0,1 М растворе меньше 3%.
Примеры слабых и сильных электролитов.
Сильные электролиты в разбавленных растворах нацело распадаются на ионы, т.е. α = 1. Но эксперименты показывают, что диссоциация не может быть равна 1, она имеет приближенное значение, но не равна 1. Это не истинная диссоциация, а кажущаяся.
Например, пусть у некоторого соединения α = 0,7. Т.е. по теории Аррениуса в растворе «плавает» 30% непродиссоцииовавших молекул. А 70% образовали свободные ионы. А электролстатическая теория дает другое определение этому понятию: если α = 0,7, то все молекулы диссоциированы на ионы, но ионы свободны лишь на 70%, а оставшиеся 30% - связаны электростатическими взаимодействиями.
Кажущаяся степень диссоциации.
Степень диссоциации зависит не только от природы растворителя и растворяемого вещества, но и от концентрации раствора и температуры.
Уравнение диссоциации можно представить в следующем виде:
AK ⇄ A- + K + .
И степень диссоциации можно выразить так:

С увеличением концентрации раствора степень диссоциации электролита падает. Т.е. значения степени для конкретного электролита не является величиной постоянной.
Так как диссоциация - процесс обратимый, то уравнения скоростей реакции можно записать следующим образом:

Если диссоциация равновесна, то скорости равны и в результате получаем константу равновесия (константу диссоциации):

К зависит от природы растворителя и от температуры, но не зависит от концентрации растворов. Из уравнения видно, что чем больше недиссоциированных молекул, тем меньше величина константы диссоциации электролита.
Многоосновные кислоты диссоциируют ступенчато, и каждая ступень имеет свое значение константы диссоциации.
Если диссоциирует многоосновная кислота, то легче всего отщепляется первый протон, а при возрастании заряда аниона, притяжение возрастает, и поэтому протон отщепляется намного труднее. Например,

Константы диссоциации ортофосфорной кислоты на каждой ступени должны сильно различаться:
I - стадия:

II - стадия:

III - стадия:

На первой ступени ортофосфорная кислота - кислота средней силы, а 2ой - слабая, на 3ей - очень слабая.
Примеры констант равновесия для некоторых растворов электролитов.

Рассмотрим пример:
Если в раствор, в котором содержатся ионы серебра внести металлическую медь, то в момент равновесия, концентрация ионов меди должна быть больше, чем концентрация серебра.
Но у константы низкое значение:
AgCl⇄Ag + +Cl - .
Что говорит о том, что к моменту достижения равновесия растворилось очень мало хлорида серебра.


Концентрация металлической меди и серебра введены в константу равновесия.
Ионное произведение воды.
В приведенной таблице есть данные:
![]()
Эту константу называют ионным произведением воды , которое зависит только от температуры. Согласно диссоциации на 1 ион Н + приходится один гидроксид-ион. В чистой воде концентрация этих ионов одинакова: [H + ] = [OH - ].
Отсюда, [H + ] = [OH - ] = = 10-7 моль/л.
Если добавить в воду постороннее вещество, например, хлороводородную кислоту, то концентрация ионов водорода возрастет, но ионное произведение воды от концентрации не зависит.
А если добавить щелочь, то повысится концентрация ионов, а количество водорода понизится.
Концентрация и взаимосвязаны: чем больше одна величина, тем меньше другая.
Кислотность раствора (рН).
Кислотность растворов обычно выражается концентрацией ионов Н + .
В кислых средах рН
<10 -7 моль/л, в нейтральных - рН
= 10 -7 моль/л, в щелочных - рН
> 10 -7 моль/л.
Кислотность раствора выражают через отрицательный логарифм концентрации ионов водорода, называя ее рН
.
рН = - lg [ H + ].
Взаимосвязь между константой и степенью диссоциации.
Рассмотрим пример диссоциации уксусной кислоты:
Найдем константу:

Молярная концентрация С=1/ V , подставим в уравнение и получим:

Эти уравнения являются законом разведения В. Оствальда , согласно которому константа диссоциации электролита не зависит от разведения растовра.
Вы никогда не задумывались над тем, почему одни растворы проводят электричество, а другие — нет? Например, всем известно, что лучше не принимать ванну, одновременно укладывая волосы феном. Ведь вода - неплохой проводник электрического тока, и если работающий фен упадет в воду, то не избежать. На самом деле, вода — не такой уж и хороший проводник тока. Есть растворы, которые проводят электричество гораздо лучше. Такие вещества называют электролитами. К ним можно отнести кислоты, щелочи и растворимые в воде соли.
Электролиты — кто они?
Возникает вопрос: почему растворы одних веществ пропускают электричество, а других — нет? Все дело в заряженных частицах — катионах и анионах. При растворении в воде электролиты распадаются на ионы, которые при действии электрического тока движутся в заданном направлении. Положительно заряженные катионы движутся к отрицательному полюсу — катоду, а отрицательно заряженные анионы движутся к положительному полюсу — аноду. Процесс распада вещества на ионы при расплавлении или растворении в воде носит гордое название — электролитическая диссоциация.
Этот термин ввел в обращение шведский ученый С.Аррениус, когда изучал свойства растворов пропускать электричество. Для этого он замыкал через раствор какого-либо вещества и следил загорается лампочка при этом или нет. Если лампочка накаливания загорается — значит раствор проводит электричество, из чего следует вывод, что это вещество является электролитом. Если лампочка остается потухшей — то раствор не проводит электричество, следовательно это вещество — неэлектролит. К неэлетролитам относятся растворы сахара, спирта, глюкозы. А вот расторы поваренной соли, серной кислоты и прекрасно проводят электрический ток, следовательно в них протекает электролитическая диссоциация.
Как протекает диссоциация?
Впоследствии теорию электролитической диссоциации развили и дополнили русские ученые И.А. Каблуков и В.А. Кистяковский, применив к ее обоснованию химическую теорию растворов Д.И. Менделеева.
Эти ученые выяснили, что электролитическая диссоциация кислот, щелочей и солей протекает в следствие гидратации электролита, то есть его взаимодействия с молекулами воды. Ионы, катионы и анионы, образующиеся в результате этого процесса будут гидратированными, то есть связанными с молекулами воды, которые их окружают плотным кольцом. Их свойства значительно отличаются от негидратированных ионов.
Итак, в растворе нитрата стронция Sr(NO3)2, а также в растворах гидроксида цезия CsOH, протекает электролитическая диссоциация. Примеры этого процесса можно выразить следующими :
Sr(NO3)2 = Sr2+ + 2NO3 -,
т.е. при диссоциации одной молекулы нитрата стронция образуется один катион стронция и 2 нитрат-аниона;
CsOH = Cs+ + OH-,
т.е. при диссоциации одной молекулы гидроксида цезия образуется один катион цезия и один гидроксид-анион.
Электролитическая диссоциация кислот происходит аналогично. Для йодоводородной кислоты этот процесс можно выразить следующим уравнением:
т.е. при диссоциации одной молекулы йодоводородной кислоты образуется один катион водорода и один анион йода.
Механизм диссоциации.
Электролитическая диссоциация веществ-электролитов протекает в несколько стадий. Для веществ с ионным типом связи, таких как NaCl, NaOH этот процесс включает в себя три последовательных процесса:
вначале молекулы воды, имеющие 2 разноименных полюса (положительный и отрицательный) и представляющие собой диполь, ориентируются у ионов кристалла. Положительным полюсом они прикрепляются к отрицательному иону кристалла, и наоборот, отрицательным полюсом — к положительному у ионов кристалла;
затем происходит гидратация ионов кристалла диполями воды,
и только после этого гидратированные ионы как бы расходятся в разные стороны и начинают двигаться в растворе или расплаве хаотично до тех пор, пока на них не подействуют электрическим полем.
Для веществ с таких как HCl и другие кислоты, процесс диссоциации аналогичен, за исключением того, что на начальном этапе происходит переход ковалентной связи в ионную за счет действия диполей воды. Таковы основные моменты теории диссоциации веществ.
Вещества-электролиты при растворении в воде распадаются на заряженные частицы — ионы. Обратное явление — моляризация, или ассоциация. Образование ионов объясняет теория электролитической диссоциации (Аррениус, 1887). На механизм распада химических соединений при расплавлении и растворении влияют особенности типов химических связей, строение и характер растворителя.
Электролиты и непроводники
В растворах и расплавах происходит разрушение кристаллических решеток и молекул — электролитическая диссоциация (ЭД). Распад веществ сопровождается образованием ионов, появлением такого свойства, как электропроводность. Не каждое соединение способно диссоциировать, а только вещества, которые изначально состоят из ионов либо сильно полярных частиц. Присутствием свободных ионов объясняется свойство электролитов проводить ток. Обладают такой способностью основания, соли, многие неорганические и некоторые органические кислоты. Непроводники состоят из малополярных или неполяризованных молекул. Они не распадаются на ионы, являясь неэлектролитами (многие органические соединения). Переносчики зарядов — положительные и отрицательные ионы (катионы и анионы).
Роль С. Аррениуса и других химиков в изучении диссоциации
Теория электролитической диссоциации обоснована в 1887 году ученым из Швеции С. Аррениусом. Но первые обширные исследования свойств растворов были проведены еще русским ученым М. Ломоносовым. Внесли вклад в изучение заряженных частиц, возникающих при растворении веществ, Т. Гротгус и М. Фарадей, Р. Ленц. Аррениус доказал, что электролитами являются многие неорганические и некоторые органические соединения. Шведский ученый объяснил электропроводность растворов распадом вещества на ионы. Теория электролитической диссоциации Аррениуса не придавала значения непосредственному участию молекул воды в этом процессе. Русские ученые Менделеев, Каблуков, Коновалов и другие считали, что происходит сольватация — взаимодействие растворителя и растворенного вещества. Когда идет речь о водных системах, то применяется название «гидратация». Это сложный физико-химический процесс, о чем свидетельствует образование гидратов, тепловые явления, изменение цвета вещества и появление осадка.

Основные положения теории электролитической диссоциации (ТЭД)
Многие ученые работали над уточнением теории С. Аррениуса. Потребовалось ее усовершенствование с учетом современных данных о строении атома, химической связи. Сформулированы основные положения ТЭД, отличающиеся от классических тезисов конца XIX века:

Происходящие явления необходимо учитывать при составлении уравнений: применить специальный знак обратимого процесса, подсчитать отрицательные и положительные заряды: они в сумме должны совпадать.
Механизм ЭД ионных веществ
Современная теория электролитической диссоциации учитывает строение веществ-электролитов и растворителей. При растворении связи между разноименно заряженными частицами в ионных кристаллах разрушаются под воздействием полярных молекул воды. Они буквально «вытягивают» ионы из общей массы в раствор. Распад сопровождается образованием вокруг ионов сольватной (в воде — гидратной) оболочки. Кроме воды, повышенной диэлектрической проницаемостью обладают кетоны, низшие спирты. При диссоциации хлорида натрия на ионы Na + и Cl - регистрируется начальная стадия, которая сопровождается ориентацией диполей воды относительно поверхностных ионов в кристалле. На заключительном этапе гидратированные ионы освобождаются и диффундируют в жидкость.

Механизм ЭД соединений с ковалентной сильнополярной связью
Молекулы растворителя влияют на элементы кристаллического строения неионных веществ. Например, воздействие диполей воды на хлороводородную кислоту приводит к изменению типа связи в молекуле с ковалентной полярной на ионную. Вещество диссоциирует, в раствор поступают гидратированные ионы водорода и хлора. Этот пример доказывает важность тех процессов, которые возникают между частицами растворителя и растворенного соединения. Именно это взаимодействие приводит к образованию ионов электролита.

Теория электролитической диссоциации и основные классы неорганических соединений
В свете основных положений ТЭД кислотой можно назвать электролит, при распаде которого из положительных ионов можно обнаружить только протон Н + . Диссоциация основания сопровождается образованием или освобождением из кристаллической решетки только аниона ОН - и катиона металла. Нормальная соль при растворении дает положительный ион металла и отрицательный — остатка кислоты. Основная соль отличается наличием двух видов анионов: ОН-группы и кислотного остатка. В кислой соли из катионов присутствуют только водород и металл.
Сила электролитов
Для характеристики состояния вещества в растворе используется физическая величина — степень диссоциации (α). Находят ее значение из отношения количества распавшихся молекул к общему их числу в растворе. Глубину диссоциации определяют разные условия. Важны диэлектрические показатели растворителя, структура растворенного соединения. Обычно степень диссоциации понижается с ростом концентрации и увеличивается при повышении температуры. Зачастую степень диссоциации конкретного вещества выражают в долях от единицы.

Классификация электролитов
Теория электролитической диссоциации в конце XIX века не содержала положения о взаимодействии ионов в растворе. Несущественным казалось Аррениусу влияние молекул воды на распределение катионов и анионов. Представления Аррениуса о сильных и слабых электролитах были формальными. Исходя из классических положений, можно получить значение α = 0,75-0,95 для сильных электролитов. В экспериментах доказана необратимость их диссоциации (α →1). Практически полностью распадаются на ионы растворимые соли, серная и соляная кислоты, щелочи. Частично диссоциируют сернистая, азотистая, плавиковая, ортофосфорная кислоты. Слабыми электролитами считаются кремниевая, уксусная, сероводородная и угольная кислоты, гидроксид аммония, нерастворимые основания. Воду также относят к слабым электролитам. Диссоциирует небольшая часть молекул Н 2 О, одновременно происходит моляризация ионов.
Теория Аррениуса включала следующие основные положения:
При растворении молекул неорганических и органических кислот, гидроксидов и солей распадаются (дисоциируют) на ионы:
HCl Н + + Cl –
NaOH
 Na +
+
OH –
Na +
+
OH –
K 2 SO 4
 2K +
+
SO 4 2–
2K +
+
SO 4 2–
Ионы представляют собой заряженные частицы, которые состоят из отдельных атомов, или из группы атомов, или из группы атомов. Предполагалось, что ионы в растворе ведут себя подобно молекулам идеального газа, т.е. не взаимодействую друг с другом.
Физические причины, которые приводят к диссоциации, в теории Аррениуса не рассматривались. Не обсуждался также вопрос о том, почему заряженные частицы, на которые должны были бы распространяться законы электростатики, не взаимодействуют друг с другом в растворе.
Диссоциация молекул на ионы является неполной, т.е. не все молекулы электролита, а лишь некоторая их доля α, названная степенью диссоциации, распадается на ионы. Степень диссоциации связанная с коэффициентом Вант-Гоффа соотношением:
α =
 (1.1)
(1.1)
где, n – число ионов, на которое распадается одна молекула электролита.
Все качественные изменения, наблюдающиеся в растворах электролитов при увеличении или уменьшении концентрации, теория электролитической диссоциации связывает с изменением степени диссоциации.
Степень электролитической диссоциации рассматривается этой теорией как одна из основных количественных характеристик раствора электролита.
Между ионами и молекулами в растворе существует равновесие. К процессу электролитической диссоциации применим закон действующих масс и второй количественной характеристикой электролита является константа диссоциации.
Ее связь со степенью диссоциации можно рассмотреть на примере бинарного электролита МА, диссоциирующего по уравнению:
МА
 М +
+ А –
М +
+ А –
и поскольку С МА = С - С α " = С(1-α),
а,
 ,
то константа электролитической
диссоциации К по теории Аррениуса должна
быть заменена следующим выражением:
,
то константа электролитической
диссоциации К по теории Аррениуса должна
быть заменена следующим выражением:
К д
= (1.2)
(1.2)
Данное уравнение было выведено В. Оствальдом и выражало сущность его закона разведения, поскольку обратная величина молярной концентрации υ = 1/С называется разведением.
Константа К д для данного электролита по теории Аррениуса является постоянной и в отличие от степени диссоциации не должна зависеть от концентрации и определяется в первую очередь природой электролита. Поэтому, используя уравнение (1.2) можно рассчитать степень диссоциации электролита в зависимости от концентрации электролита.
Решая квадратное уравнение и учитывая, что α>0, получим:
α =
 (1.3)
(1.3)
И как следует из уравнения (1.3), при С → 0 или К → ∞, α → 1 т.е. электролит становится полностью диссоциированным.
С другой стороны, при малых константах диссоциации и при не очень низких концентрациях электролита, когда К 2 << 4КС
α ≈
 (1.4)
(1.4)
Соотношения (1.2) и (1.4) применимы только для бинарных электролитов.
4.1.3 Ионное равновесие в растворах электролитов
Теория Аррениуса позволила объяснить многие химические особенности растворов электролитов.
На ее основе было дано первое научное определение понятием «кислота» и «основание» согласно которым кислота (НА) это водородосодержащее соединение при диссоциации которого образуются ионы водорода, а основание – соединение, (МОН), при диссоциации которого образуются ионы гидроксила
HА
 Н
+ +
А –
Н
+ +
А –
МOH
 М + +
OH
–
М + +
OH
–
Это дало возможность рассматривать реакцию нейтрализации, как процесс взаимодействия ионов водорода кислоты и гидроксид иона основания с образованием воды, а в разбавленных растворах сильных кислот и сильных оснований, для которых была установлена их полная диссоциация, характеризоваться постоянным тепловым эффектом независимо от природы кислот и оснований.
Для процессов диссоциации кислоты НА и основания МОН закон Освальда можно записать в виде (1.2), где К д обозначает так называемую концентрационную константу кислоты (К А) или основания (К В)
К А
= (1.5)
(1.5)
К В
= (1.6)
(1.6)
Их значение определяется равновесными концентрациями. Так как константы обычно имеют довольно большие численные значения, то их удобно записывать в логарифмической шкале:
рК А = - lg K A
рК В = - lg K В (1.7)
Понятие константы равновесия может
быть применимо непосредственно и к
растворителям, молекулы которых способны
распадаться на ионы. Например,
концентрационную константу равновесия
реакции диссоциации воды: H 2 О Н + +OH
-
Н + +OH
-
К Д
= (1.8)
(1.8)
Но так как очень незначительная часть молекул воды распадается на ионы, можно считать, что концентрация воды практически постоянна, тогда получим:
 =
(1.9)
=
(1.9)
Где, константа
 ,
зависящая от температуры, называется
ионным произведением воды. При 20 - 25 0 С
,
зависящая от температуры, называется
ионным произведением воды. При 20 - 25 0 С
р = - lg
= - lg ≈ 14
≈ 14
Следовательно, при этой температуре концентрации ионов водорода и гидроксид-ионов в чистой воде, а также в любом водном растворе электролита имеющим нейтральную реакцию, равны 10 -7 моль/л. Концентрацию ионов водорода, также принято выражать в логарифмической шкале, обозначая логарифм концентрации ионов водорода, взятый со знаком минус, символом рН.
рН = - lg

Наличие, хоть и очень небольших, концентраций ионов, образующихся при диссоциации растворителя, привод к их взаимодействию с ионами растворенных в данном растворе веществ и возникновению новых ионных равновесий. Это явление в общем случае называется сольволиз , а если растворитель – вода, тогидролиз .
Для соли слабой кислоты и сильного
основания реакция гидролиза протекает
по уравнению А - +H 2 О НА + ОН - и характеризуется константой
гидролиза.
НА + ОН - и характеризуется константой
гидролиза.
К Г
= (1.10)
(1.10)
Поскольку
 =
const. Используя уравнения (1.5.) и (1.9) можно
записать
=
const. Используя уравнения (1.5.) и (1.9) можно
записать
К Г
=
 (к-ты) (1.11)
(к-ты) (1.11)
Уравнение (1.11) показывает, что константа гидролиза тем больше, чем слабее кислота. Подобное соотношение можно получить и для гидролиза соли сильной кислоты и слабого основания. Уравнение гидролиза имеет вид
М +
+ H 2 О
 МОН + ОН +
МОН + ОН +
а константа гидролиза
К Г
= (осн.) (1.12)
(осн.) (1.12)
Вследствие зависимости
 от температуры с ростом последней
заметно возрастают константы гидролиза.
от температуры с ростом последней
заметно возрастают константы гидролиза.
Следует также отметить, что в первом случае раствор будет иметь щелочную реакцию (рН > 7), а во втором – реакция раствора будет кислая (рН < 7).
Из сказанного ясно, что в случае растворения в воде соли сильной кислоты и сильного основания нейтральная реакция среды должна сохраняться.
Растворы, содержащие слабые кислоты и соли, образованные этими кислотами и сильными основаниями, или содержащие слабые основания и соли, образованные этими основаниями и сильными кислотами, обладают замечательным свойством противостоять изменению рН при добавлении к ним кислот или оснований. Это свойство называется буферным свойством растворов , а растворы, обладающие им –буферными растворами .
Рассмотрим водный раствор, содержащий уксусную кислоту и ацетат натрия. Добавим к этому раствору сильное основание, например гидроксид натрия. Произойдет реакция нейтрализации NaOH слабой кислотой.
СН 3 СООН + Na + + ОН – = СН 3 СОО – + Na + +Н 2 О
Благодаря чему кислотность раствора практически останется неизменной или изменится во много раз меньше, чем если бы мы добавили NaОН к раствору ацетата натрия.
Если же к буферному раствору добавить сильную кислоту, например НСl, то произойдет реакция взаимодействия с ацетатом натрия
СН 3 СОО – + Na + + Н + + Сl – = СН 3 СООН + Na + +Сl –
с образованием недиссоциированных молекул уксусной кислоты, т.е. с поглощением ионов водорода.
Изменение концентрации ионов водорода буферного раствора в результате добавки кислого или щелочного реагента рассчитать можно следующим образом.
Записывают константу равновесия уксусной кислоты
К к
= (1.13)
(1.13)
В этом уравнении концентрация недиссоциированных молекул очень слабо диссоциирующей уксусной кислоты практически равна аналитической концентрации кислоты (Ск), а концентрация ацетат-ионов равна аналитической концентрации полностью диссоциирующего ацетата натрия (Сс). Тогда
 =
= (1.14)
(1.14)
История открытия такого интересного явления в химии как электролитическая диссоциация началась в 1887 году, когда шведский химик Сванте Аренниус во время исследований электропроводности водных растворов, высказал предположение, что в подобных растворах вещества могут распадаться на заряженные частицы – ионы. Ионы эти пребывают в движении, передвигаясь к электродам, как положительно заряженному катоду, так и отрицательно заряженному аноду. Этот процесс распада и получил название электролитической диссоциации, именно он является причиной появления электрического тока в растворах.
Теория электролитической диссоциации
Классическая теория электролитической диссоциации, разработанная первооткрывателем С. Аренниусом совместно с В. Освальдом, прежде всего, предполагала, что распад молекул на ионы (собственно диссоциация) происходит под действием электрического тока. Впоследствии выяснилось, что это не совсем так, поскольку было выявлено существование ионов в водных растворах, независимо от того, проходил через них ток или нет. Тогда Сванте Аренниус сформировал новую теорию, суть ее заключается в том, что электролиты самопроизвольно распадаются на ионы под воздействием растворителя. А уже наличие ионов создают идеальные условия для электропроводности в растворе.

Примерно так выглядит электролитическая диссоциация схематично.
Большое значение электролитической диссоциации в растворах заключается в том, что она позволяет описывать свойства кислот, оснований и солей, и далее мы детально на этом остановимся
Электролитическая диссоциация кислот
Н 3 РО 4 ⇄ Н + Н 2 РО- 4 (первая ступень)
Н 2 РО 4 ⇄ Н + НРO 2 - 4 (вторая ступень)
Н 2 РО 4 ⇄ Н+ PО З - 4 (третья ступень)
Так выглядят химические уравнения электролитической диссоциации кислот. В примере показана электролитическая диссоциация фосфорной кислоты Н 3 РО 4 которая распадается на водород H (катион) и ионы анодов. Причем диссоциация много основных кислот проходит, как правило, только по первой ступени.
Электролитическая диссоциация оснований
Основания отличаются от кислот тем, что при их диссоциации в качестве катионов образуются гидроксид-ионы.
Пример уравнения химической диссоциации оснований
KOH ⇄ K + OH-; NH 4 OH ⇄ NH+ 4 + OH-
Основания, которые растворяются в воде, называют щелочами, их не так уж и много, в основном это основания щелочных и щелочноземельных , таких как LiOH, NaОН, КОН, RbОН, СsОН, FrОН и Са(ОН) 2 , Sr(ОН) 2 , Ва(ОН) 2 , Rа(ОН) 2
Электролитическая диссоциация солей
При электролитической диссоциации солей в качестве катионов образуются металлы, а также катион аммония NH 4 , а анионами стают кислотные остатки.
(NH 4) 2 SO 4 ⇄ 2NH+ 4 + SO 2 - 4 ; Na 3 PO 4 ⇄ 3Na + PO 3- 4
Пример уравнения электролитической диссоциации солей.
Электролитическая диссоциация, видео
И в завершение образовательное видео по теме нашей статьи.
Цветовая гамма